生命编码背后的故事(十一)
分子结构
1862年初的一个夜晚,德国化学家凯库勒(August Kekule)正在家里写作教科书,却在壁炉的温暖中打起了盹。他看到许多原子手牵手连成长串在火光中舞动,像是一堆蠕动着的蛇。其中一条蛇咬住自己的尾巴,形成一个圆环在他眼前转动着。凯库勒猛然惊醒。他已经不止一次做这样的梦了。但这次,他终于看清了那只头尾相连的蛇,领悟到那正是苯分子的形状。
苯是一种简单的有机化合物。它的分子相对很小,只有六颗碳原子和六颗氢原子(C₆H₆)。物理学家法拉第早在1825年研究燃油废料时分离出这个化学品。其后几十年里,化学家绞尽脑汁也没能猜想出那12颗原子是怎样的一个组合。
古希腊的德谟克利特提出世界万物均由不可再分的原子组成时,他也必须将分离的原子结合起来构成自然界的日常物质。于是他设想原子有着不同的形状。金属原子带有坚硬的钩子,相互套牢成为固体。水的原子比较滑润,空气的原子则轻灵好动,等等。
拉瓦锡在18世纪末以实验证明水由氢和氧组成,既非元素也不是原子。在道尔顿的现代原子论基础上,化学家假定原子之间存在一种“亲和力”(affinity),互相吸引而结合成五花八门的分子。因为这个亲和力,氢原子和氧原子被束缚在一起,形成“化学键”(chemical bond)。水分子相当稳定,就是因为这个化学键比较结实。
不同原子之间的亲和力大小不同,形成的化学键也强弱不一。这样分子相遇时其化学键必须经受来自其它原子亲和力的考验。比较弱的键会被打开,由新的、更强的化学键取代。这个过程就是化学反应:分子中的原子重新组合成新的分子。催化剂也正是因为自身的存在改变了其它分子中亲和力的分布而起到协助化学反应发生的作用。
虽然用词更为现代化,亲和力、化学键的概念其实与德谟克利特的钩子大同小异,都属于盲目的猜测。与拉瓦锡同时代的德国哲学家康德(Immanuel Kant)在1786出版的《自然科学的形而上学基础》1前言中感叹,“化学最多只会成为一门系统的艺术或实验学说,但永远不可能是真正的科学。”2他心目中的“真正科学”是以伽利略、牛顿为代表的动力学。而化学研究的对象过于棘手,没法同样地以精确的数学表述。
在凯库勒的19世纪中叶,亲和力也已经有了更为定量的发展,具体为元素的“价”(valence)。每个元素都被明码标价,相当于它拥有的钩子数目3。当分子中每颗原子的钩子都与另一颗原子的钩子相连时,它们便形成稳定的分子。这样互相连接好的钩子叫做“共价键”(covalent bond)。比如氢为一价,氧为二价。于是一颗氧原子会同时勾住两颗氢原子,形成稳定的水分子(H₂O)。一颗氢和一颗氧组合时就不成其为分子,它们还有着一个剩余的钩子。那正是表征酒类的羟基(-OH),也有着一价。因此羟基会再与另外一价的原子或基结合,形成稳定的(酒类)分子。
也是在19世纪后期出现的元素周期表就是这类化学性质的规律性体现。在表中同一个纵列(“族”)的元素有着相同的价。
碳是四价元素。一颗碳原子因而可以与两颗氧组成二氧化碳(CO₂),或者与四颗氢组成最简单的有机物甲烷(CH₄)。在这些分子里,碳的钩子分别与氧或氢的钩子两两相连,其结构一目了然。
甲烷是碳氢化合物,属于完全由碳与氢组成的“烃”(hydrocarbon),是天然气的主要成分。与作为碳水化合物的糖分子一样,烃分子可大可小。只有一颗碳的甲烷最小,下一个是乙烷(C₂H₆),有着两颗碳、六颗氢。以此类推,烃分子可以有任意数目的碳及相应的氢,即使成百上千也不以为奇。
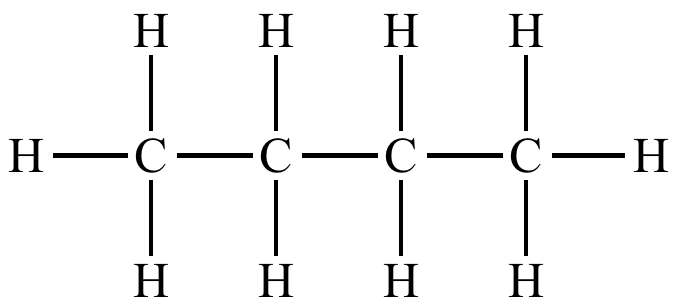
幸运的是烃分子的结构不随其原子数目的增多而变得过于复杂。它们有着直截了当的构造:像凯库勒的梦中的蛇,碳原子互相牵着手形成一条链,它们另外两个钩子则分别连上氢原子。如此这般,任意大小的烃分子在结构上如出一辙,其碳和氢的比例也就有着清晰的规律:每颗碳原子带着两颗氢,另外还有两颗额外的氢原子为碳链的两端“收尾”。
苯也是由碳和氢组成,因而也属于烃类。但它那各有六颗的碳和氢的成分却违反了这个既定安排。凯库勒和他的同行们没有得手的工具,只能像拼接七巧板一般猜想分子的结构,以让每个原子的钩子都有所归属为终极目标。然而,那六个氢钩子与24个碳钩子的几何游戏却让所有化学家费尽心机也无法安排得妥妥帖帖。就连凯库勒也还是在前后长达七八年的反复梦境之后才幡然醒悟:苯那六颗手牵手的碳原子不是一字排开,而是像那条咬著自己尾巴的蛇一样首尾相连形成一个环。除了彼此手拉手,它们之间还共享着三个共价键。这样所有的钩子才得以连接,成为稳定的分子4。
苯分子结构的成功解析不仅终于击碎难倒化学家几十年的绊脚石,也为有机化学打开一个更为丰富多彩的新天地。无论烃、糖、酒还是脂肪,绝大多数有机大分子由碳、氢、氧等几个简单元素以不同比例组成。它们都是以手拉手的碳链为骨干,在其上再挂上不同的原子或基。有了凯库勒的突破,碳链不再只是单调的一条直线,还可以形成各种各样的环。这么一来,分子的结构变得格外地多样化。即使分子式完全相同,“同一个”分子往往也会以不同的结构出现,叫做“同分异构体”(isomer)。它们会表现出完全不同的物理、化学性质,在生物的代谢过程中扮演迥然相异的角色。
记录原子构成的分子式因而不足以表达这些化学品的区别。为弥补这一缺陷,费舍尔在1891年发明一种以他命名的“费舍尔投影”5,将分子的三维结构像画地图一样描绘在二维的纸面上。这就是今天化学教科书上常见的分子结构图。它可以表示出异构体中的细微区别,包括左右互换时的“手性不对称”(chirality)。
费舍尔那时已经是知名的有机化学家。20年前,当他还是柏林大学的新生时,德国在战争中赢得法国割让的阿尔萨斯地区。凯库勒的学生拜尔(Adolf von Baeyer)受聘,与霍普-塞勒一起前往斯特拉斯堡大学组建全球领先的生物化学系,彰显德国的科学实力。费舍尔也随大流转学到那里成为拜尔的学生。在1874年获得博士学位后,他留校继续研究化学。那时,他的注意力集中在糖类的分子结构和性质。
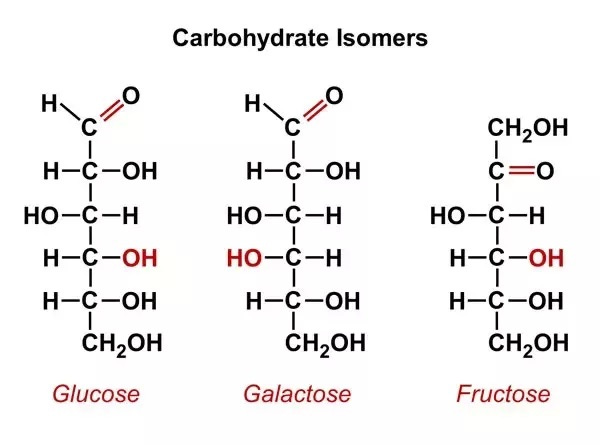
与烃一样,糖分子的主干也是碳链,只是与碳相连的氢中有些被置换为同为一价的羟基。它们也有着花样繁多的同分异构体。比如植物在光合作用中合成的葡萄糖就是有着六颗碳原子的单糖——“己糖”(C₆H₁₂O₆)——的多种异构体之一,另外还有水果等食物中常见的果糖(fructose)等等。它们的碳链既可以是直线,也可以头尾相连成一个环。费舍尔在实验中发现、发明并提纯各种试剂检验这些异构体的区别,同时选取合适的催化剂人工分解、合成这些有机分子。
在用他的投影图描绘不同分子结构的同时,费舍尔察觉同一分子的异构体会表现出不同的化学性质正是因为其内部原子有着不同的位置分布和几何形状。正像一把锁,只要锁芯内的机关有些许改变,原来的钥匙就无法打开,需要更换新钥匙。己糖不同的异构体互相之间也只存在微小的差异,能够将其中一种发酵为酒的催化剂对另一种就无动于衷:它在那里已经不再是合适的钥匙。
推而广之,费舍尔发现这是有机化学中的普遍现象。切割蛋白质的酶也有着同样的“一把钥匙开一把锁”特性。他的兴趣随即也跟着转往那个时代更为热门的蛋白质。
1902年9月22日,已经有80年历史的德国自然科学家和医生学会在捷克风景秀丽的度假胜地卡尔斯巴德召开年度大会。那天上午,布拉格出生、也已经转到斯特拉斯堡大学任职的生理学家霍夫迈斯特(Franz Hofmeister)发表一个出乎意料的发现:蛋白质就是由氨基酸组成的一条长链。
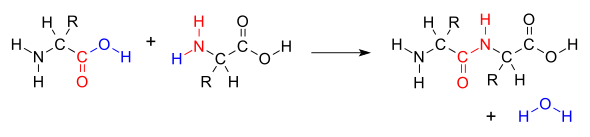
硕大的蛋白质分子在动物肠胃消化时被那里的酶切割为小巧的氨基酸分子早已为生理化学家了解。但霍夫迈斯特更进了一步。他指出同时拥有着氨基和羧基的氨基酸是大自然为蛋白质准备好的积木块。一个氨基酸分子的氨基会与另一个氨基酸分子的羧基发生反应。它们原有的化学键被打破,在氨基(-NH₂)失去一颗氢,羧基(-COOH)失去一颗氢和一颗氧之后,剩余的原子连接形成新的化学键。两个氨基酸因此组合成为一个新分子。而那被遗弃的两颗氢和一颗氧也相互抱团,成为水分子析出。这样,氨基酸如此组合时会失去水分,属于脱水反应。
一边是氨基另一边是羧基的氨基酸因而是两头正好互为匹配的积木块,可以通过连续的脱水缩合像碳原子一样彼此手拉手形成一条长链。那就是蛋白质。酶对蛋白质的切割正是将连接这条长链的化学键重新打开、恢复氨基酸原形的逆向过程。
霍夫迈斯特的讲解立刻引起全场轰动,但最为惊讶的莫过于费舍尔。他被会议安排在当天下午发言,而他准备好的内容与霍夫迈斯特毫无二致。他们两人互不知情,同时做出了同样的发现。但与霍夫迈斯特纸上谈兵,靠逻辑推理得出这一结论相反,费舍尔的结果来自细致全面的实验,更为切实可靠。
费舍尔也已经将两个氨基酸结合而成的新分子命名为“肽”(peptide)。与施旺发现的胃蛋白酶一样,这个名字来自希腊语的“消化”。新分子中形成的化学键相应地成为“肽键”,而多个氨基酸结合后的分子也叫做“多肽”(polypeptide)。那是蛋白质的雏形。
因为各种各样的氨基酸都有着同样的氨基和羧基,它们是有着相同钩子的不同积木块,可以任意组合,搭建出五花八门名目繁多的蛋白质。
那时候也在钻研蛋白质结构的科赛尔没能做出这个重大发现。他只好再度将目光转回已经被改名为核酸的核素,试图解析——猜测——出这个神秘化合物的结构。
1884年时,费舍尔在动物的尿液里分离出一种新的化学品。他将其命名为“嘌呤”(purine),意为“纯尿”。像大多数有机物一样,嘌呤后来成为一类化合物的统称。咖啡、茶和可可中所含的咖啡因就是其中之一。几年以后,费舍尔成功地像合成糖分子一样人工合成了咖啡因。
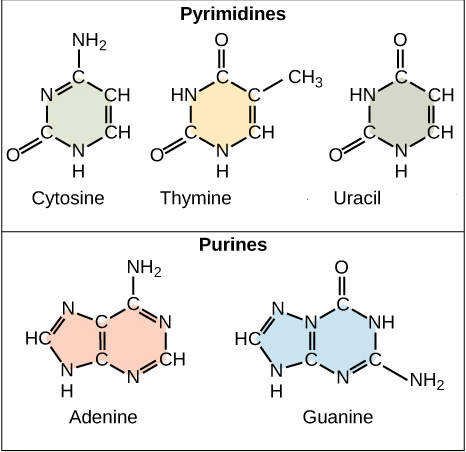
科赛尔在核酸中也发现了嘌呤。那是他已经分离出的五种碱中的两种:腺嘌呤(adenine)和鸟嘌呤(guanine)。另外三种碱则属于与嘌呤关系很近的“嘧啶”(pyrimidine),分别为胸腺嘧啶(thymine)、胞嘧啶(cyrosine)和尿嘧啶(uracil)6。
在科赛尔和其它实验室的协同努力下,这些化合物的成分和结构在19世纪末陆续被解析。它们都由碳、氢、氮和氧原子组成,具备极为接近的化学性质。较为简单的嘧啶有着与苯相同的环状结构,只是环链中两个碳原子被氮原子替代。嘌呤稍微复杂一些,它们的环还紧连着另一个稍小一点的五边环。
这些碱分子比氨基酸简单,却不像氨基酸那样有着现成的钩子可以方便地互相连接成为长链。它们也不含有核酸中相比蛋白质更为显著的磷元素。显然,核酸不像蛋白质那样只是这些碱分子直接相连而成的大分子。
科赛尔也在实验中看到一些蹊跷。从各种动物内脏、精子、血液等组织中分离出的核酸只含有腺嘌呤、鸟嘌呤、胞嘧啶和胸腺嘧啶,没有尿嘧啶。而来自酵母细胞中的核酸却有着腺嘌呤、鸟嘌呤胞嘧啶和尿嘧啶,独缺胸腺嘧啶。在这些碱被分别提取之后,核酸中的磷以磷酸盐(phosphate)的形式剩余下来。剩余物中还有一种过去从未见过的糖。与葡萄糖和果糖那些有六颗碳原子的己糖不同,这是一种只有五颗碳原子的“戊糖”(C₅H₁₀O₅)。面对这一大堆毫不相干的积木块,科赛尔束手无策,无法解开它们如何搭建出核酸这个谜。
在1902年的大会上提出蛋白质结构后,费舍尔在那年年底赢得诺贝尔化学奖。那是这个随新世纪而来的大奖的第二次颁发。他得奖的成就并非蛋白质,而是更早对糖和嘌呤的研究和合成。三年后,他的导师拜尔在1905年获得同样的殊荣。接着,1907年的诺贝尔化学奖颁发给证明酵母的发酵能力不依赖生命活力的比希纳。短短几年间,新兴的生物化学已经多次得到这个正在成为科学界最高奖的首肯。
19世纪堪称化学的黄金时代。从道尔顿的原子论到门捷列夫的元素周期表,从规模惊人的化肥、化工企业到生命体内细胞中的代谢,化学无处不在,成绩斐然。当诺贝尔在世纪末设立这个奖项时,他毫不犹豫地选择了物理和化学——两个在工业革命中持续为人类造福的实用科学。
他没有选择生物学。那个年代的生物学还着重于标本的收集和分类,与人类的福祉没有直接关系。对化学的前途深为悲观的康德对生物学更是彻底失望。他在1790年出版的《判断力批判》7中断言:“永远不会出现草叶中的牛顿,因为人类的科学永远无法解释生命如何能从无生命的物体中出现。8”
在物理和化学之外,诺贝尔选取了对人类生存、健康不可或缺的医学和生理学,合在一起成为另一个科学奖项。从1901年开始,诺贝尔生理学或医学奖连年颁发给与治病救人息息相关的医学成就。直到1910年,这个奖被授予做出“在蛋白质和细胞核物体研究中的贡献”的科赛尔。虽然所得的是生理学或医学奖,科赛尔的成就也属于生物化学的范畴。以诺贝尔奖委员会提供的获奖缘由而言,这个奖似乎更属于米歇尔。不幸的是米歇尔已经在1895年英年早逝。诺贝尔在遗嘱中明确规定获奖者必须是活着的人选。
在布赫那获奖之后的1908年,诺贝尔化学奖也剑走了偏锋,授给物理学家卢瑟福(Ernest Rutherford)。那是一次阴错阳差的运作,让卢瑟福啼笑皆非。9作为20世纪初的物理学家,卢瑟福喜欢自吹只有物理学才是真正的科学。化学、生物等学科的研究工作不过只是忙忙碌碌地在“集邮”。
的确,即使化学在19世纪有了突飞猛进的发展,它依然缺乏“真正科学”的根基。无论是亲和力、价还是化学键,它们都还只是德谟克利特式的凭空想象,没有切实的根据或逻辑。
卢瑟福那时也没意识到,作为“真正科学”的化学在那个新世纪已然呼之欲出,即将在他自己的实验室里破土发芽。
(待续)
Metaphysical Foundations of Natural Science
Chemistry can become nothing more than a systematic art or experimental doctrine, but never a science proper.
个别元素可以有不止一个价,或者钩子的数目会变化。
与科学史上各种典故一样,凯库勒多年之后才讲述的梦境故事是否可信也充满争议。类似环形的分子模型在他之前已经有人提出,但凯库勒完整解决苯分子结构的优先权没有争议。
Fischer projection
这些名称源于它们最早被发现时的来历。比如鸟嘌呤首先是从鸟粪中被分离而出。
Critiques of Teleological Judgement
There will never be a Newton for the blade of grass, because human science will never be able to explain how a living being can originate from inanimate matter.



carlsbad 不在海边,是不是有个湖不肯定;bad 就是英语 bath 有温泉的旅游景点